三、在美国临床试验注册中心进行临床试验注册
在线申报全部注册程序(网址:https://clinicaltrials.gov/)
1. 申请PRS账号
在注册临床试验之前,有必要使用协议注册系统(PRS)帐户登录(图12-11)。
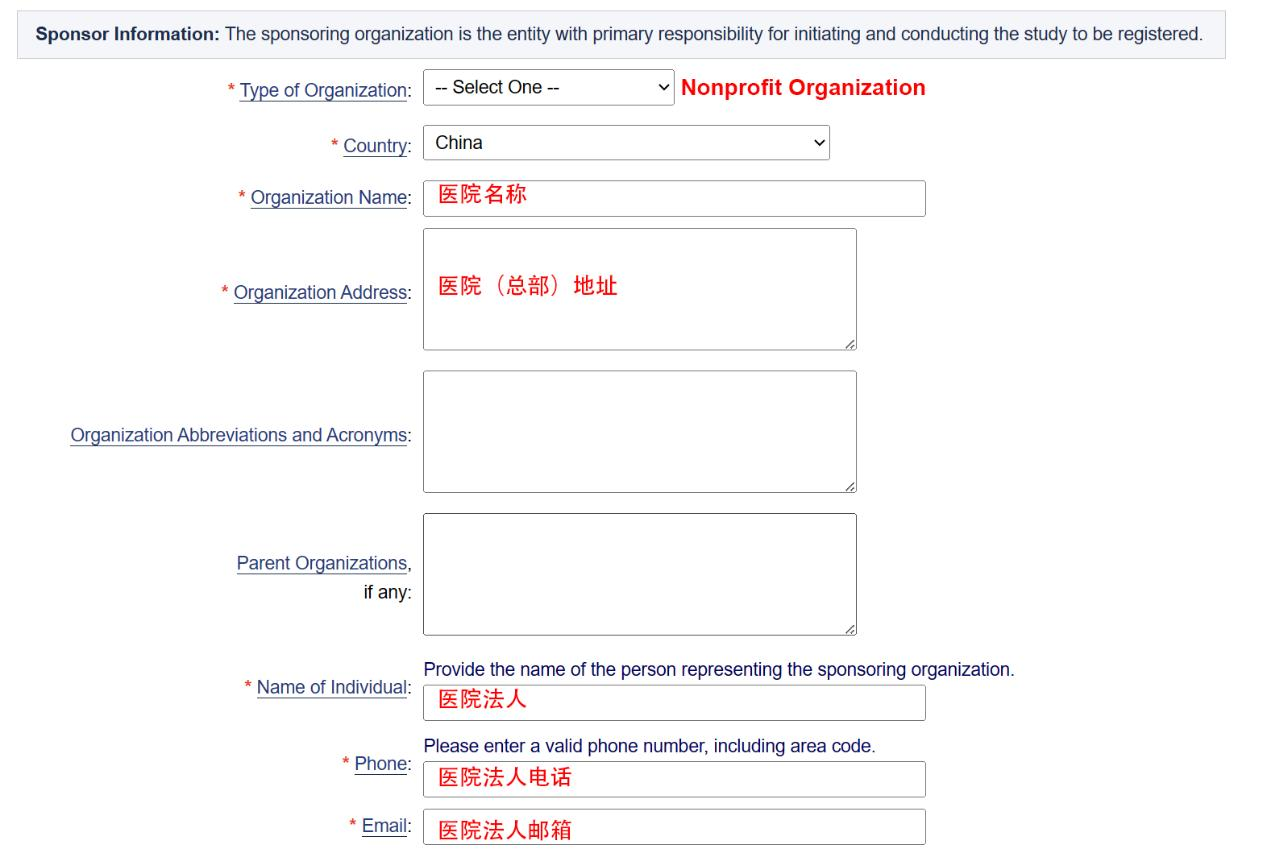
图12-11 申请PRS账号
PRS账户有两种类型:一种是单位账户(如公司、大学、医疗机构等),也推荐使用。临床研究人员可以了解他们的医疗机构是否申请了临床试验账户(通常可用),联系相关负责人,收到自己的账户和密码,登录后直接创建临床试验项目。另一种类型是个人账户,不推荐使用。如果上级组织没有临床帐户,请将其提交至https://www.clinicaltrials.gov/ct2/apply-account-org。以医院为例,在接受条件后,首先输入医院信息(*为必填字段)。
2. 然后填写账户管理人和监管机构信息(图12-12)

图12-12 填写账户信息
3. 填写账户管理人和监管机构信息界面
点击Submit Application。在申请后的3-5个工作日,账号将通过电子邮件形式告知申请者。
4. 临床试验方案注册
(1)Study Identification 研究鉴定;
(2)Study Status 研究现状;
(3)Sponsor/Collaborators 实验赞助商/合作者;
(4)Oversight 对于临床试验研究,对于 FDA 注册的标准化干预措施,需要填写是否为801个临床试验以及是否将登记信息延迟公开。如果申请注册的研究有经 FDA 批准的临床试用新药申请或临床器械研究豁免(Investigational Device Exemption, IDE),则需填写 IND/IDE 序列号和此序列号的颁发部门;
(5)Description 试验摘要(必填)以及对试验进行简单阐述;
(6)Condition 实验条件;
(7)Study Design 若为干预性研究,需填写研究目的(Primary Purpose)、研究阶段(Study Phase)、干预模型(Intervention Model)、分组数(Number of Arms)、盲法(Masking)、干预分组方式(Allocation)、受试对象数目(Enrollment)、研究终点(Study Classification)等方面内容。如果为观察性研究,则需填写模型种类(Observational Study Model),观察时间点(Time Perspective),生物标本存放形式(Biospecimen Retention),受试者数目和分组数目(Number of Groups/Cohort)等内容;
(8)Groups and Interventions 试验分组的名称和类型。若为干预性研究,需要注意的是干预类型(Intervention Type)和名称(Intervention Name)是必须填写的项目,并进一步详细说明;
(8)Outcome Measures对试验主要结局和次要结局进行描述;
(9)Eligibility 实验资格;
(10)Contacts/Locations填写各试验中心的名称、地址以及人群招募情况,同时填写研究者的相关信息等;
(11)为研究提案填写参考文献和相关网站链接,参考文献需要提供 PMID 编号或文献索引,如果是网站,请提供准确的网址和说明。在填完所有单元信息后,点击“Complete”,还需依次点击“Approve”和“Release”,将有专业的 Review Staff 研究方案进行审查,审查合格后,对通过的临床注册方案进行公开,系统里状态更新为 Public。
四、两种注册的选择
当准备发表英文期刊时,两者选其一进行注册即可。中国临床实验注册中心是被顶级期刊和其他期刊认可的正规注册平台。并且同一项研究在一个注册平台注册一次即可。
参考文献
[1] 崔月婷, 张迪, 刘菲. 医药卫生期刊临床试验注册现状及问题分析[J]. 今传媒, 2024, 32(1): 67-70.
[2] 杨星月, 刘佳, 何丽云, 等. 病例注册登记研究的应用进展[J]. 中国循证医学杂志, 2016, 16(12): 4.
[3] 米娜瓦尔·阿不都, 郝园, 孔翔瑜, 等. 中国临床试验注册10年:现状与问题[J]. 中国询证医学杂志, 2018, 18(06): 522-525.
[4] 宗欣, 董江萍, 陶秀梅. 对我国临床试验登记注册和信息共享的思考与建议[J]. 中国新药杂志, 2015, 24(21): 4.
[5] 国家口腔疾病临床医学研究中心 临床研究注册与备案常见问题. https://mp.weixin.qq.com